リンクメッドとは2023年12月に戦略的提携を行い(リンク)、64Cu-ATSMの国内での将来的な商業化はPDRファーマが中心となって進めます。
国立がん研究センターで実施されていた、悪性脳腫瘍の患者さんを対象としたフェーズ1試験(医師主導治験)が完了し、その結果がASCO(米国臨床腫瘍学会)で発表されました。
フェーズ1試験の結果を安全性・有効性の面から検証した結果、次のステップに進めるということで、2024年6月からフェーズ3試験を開始しました。
有効性についてもう少し詳しくご説明すると、膠芽腫という神経膠腫の中でも悪性のがんの患者さんにおいて、9名のうち5名が1年以上生存されたということです。一般的には再発した膠芽腫の患者さんの1年以上の生存率は30~40%と言われています。64Cu-ATSMは有効な治療効果が期待される可能性があると考えられました。
今回のフェーズ3試験は医師主導治験として国立がん研究センターで開始され、これまでの標準治療と比較して64Cu-ATSMが生存期間を延長するかどうかを検証する比較試験となります。対象となる患者さんは悪性神経膠腫(※)と診断された患者さんです。
リンクメッドは、フェーズ1試験の治験薬を提供したQST(国立研究開発法人 量子科学技術研究開発機構)からスピンアウトしたQST認定ベンチャーで、フェーズ3試験において治験薬を提供するという役割を担います。
64Cu-ATSMの開発が一歩前に進んだというのは素晴らしい進捗です。フェーズ3試験が順調に進むことを期待しています。
※神経膠腫とは、神経膠細胞という脳・脊髄を構成する細胞が悪性化したもので、非常に多くの種類があります。今回のフェーズ3ではさらにその中でも悪性・難治性神経膠腫と診断された患者さんに対して実施されます。
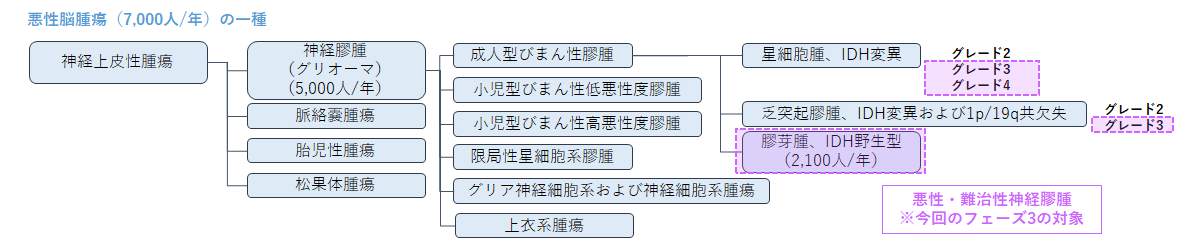
がん情報サービス(https://ganjoho.jp/public/cancer/glioma/about.html)より

ペプチドリーム広報の沖本です
生命工学系の大学院を卒業後、出版社、証券会社をへて2020年にペプチドリームに入社しました。わかりやすくリリース内容や技術内容をお伝えしていきたいと思いますのでよろしくお願いいたします。

