Alnylam社との共同研究は2021年に開始され、ペプチドリームのペプチド創薬技術と、Alnylam社の核酸医薬領域の専門性を合わせ、核酸-PDCの創製を行ってきました。下図のような、ペプチドとsiRNAを結合させた構造となっており、細胞表面の標的に結合し、細胞内に取り込まれることでsiRNAが薬効を発揮します。
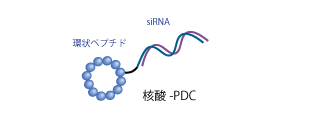
核酸-PDCの構造
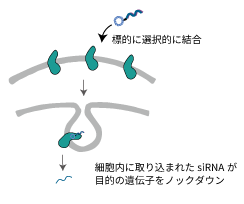
核酸-PDCの働き
siRNAはRNAiという現象を利用した薬剤で、標的のmRNAを分解することで特定の遺伝子の発現を抑える短いRNAです。siRNAが遺伝子の発現量を減らす効果は「ノックダウン」と呼ばれ、高い効果と特異性があることが知られています。細胞内にある標的のRNAに結合してその作用を発揮するので、既存の低分子医薬品や抗体医薬では標的とすることが難しい(いわゆるundruggable)とされている標的にもアプローチできる治療法であることから、多くの製薬企業がこの核酸医薬品の研究開発に注力しています。siRNAは細胞内に入るとこのノックダウン効果を発揮するのですが、そのためには目的の組織に正確・効率的にデリバリーする必要があります。
一方、ペプチドは、目的とする標的に対して選択的に結合するという特徴を持っています。ペプチドと核酸を組み合わせることにより、両者の長所が活きる、理想的なモダリティが作られるのです。
Alnylam社は世界で最初に承認されたRNAi治療薬を開発・販売しているこの領域のパイオニア企業です。デリバリーでも独自技術を保有しており、特に、肝臓に対して受容体を介して特異的にデリバリーを行うGalNAc技術を持っています。(参考ページ)
一方で、肝臓以外の組織へのデリバリーする技術が確立していないことがこれまでの課題でした。今回両社共同で、肝臓以外の組織を標的とした薬剤の創製を行い、動物モデルで目的の細胞に取り込まれ、標的遺伝子を顕著にノックダウンするという狙い通りの結果を得ることができました。
ペプチドリームのPDPS技術を用いると、さまざまな標的にたいして選択的に結合するペプチドを創製できるため、さまざまな組織へのデリバリーが可能になることが期待できます。また、デリバリーするsiRNAについて、様々な配列に対応することが可能です。つまり、今回の結果は特定の細胞に特定のsiRNAを送達できることを示した内容でしたが、同じアプローチを横展開することにより、さまざまな組織にさまざまなsiRNA遺伝子を送達することが可能になると考えられます。
この、拡張性について、プレスリリースでは「モジュール型の治療プラットフォーム」と表現させていただきました。
モジュール型治療プラットフォームのイメージ図
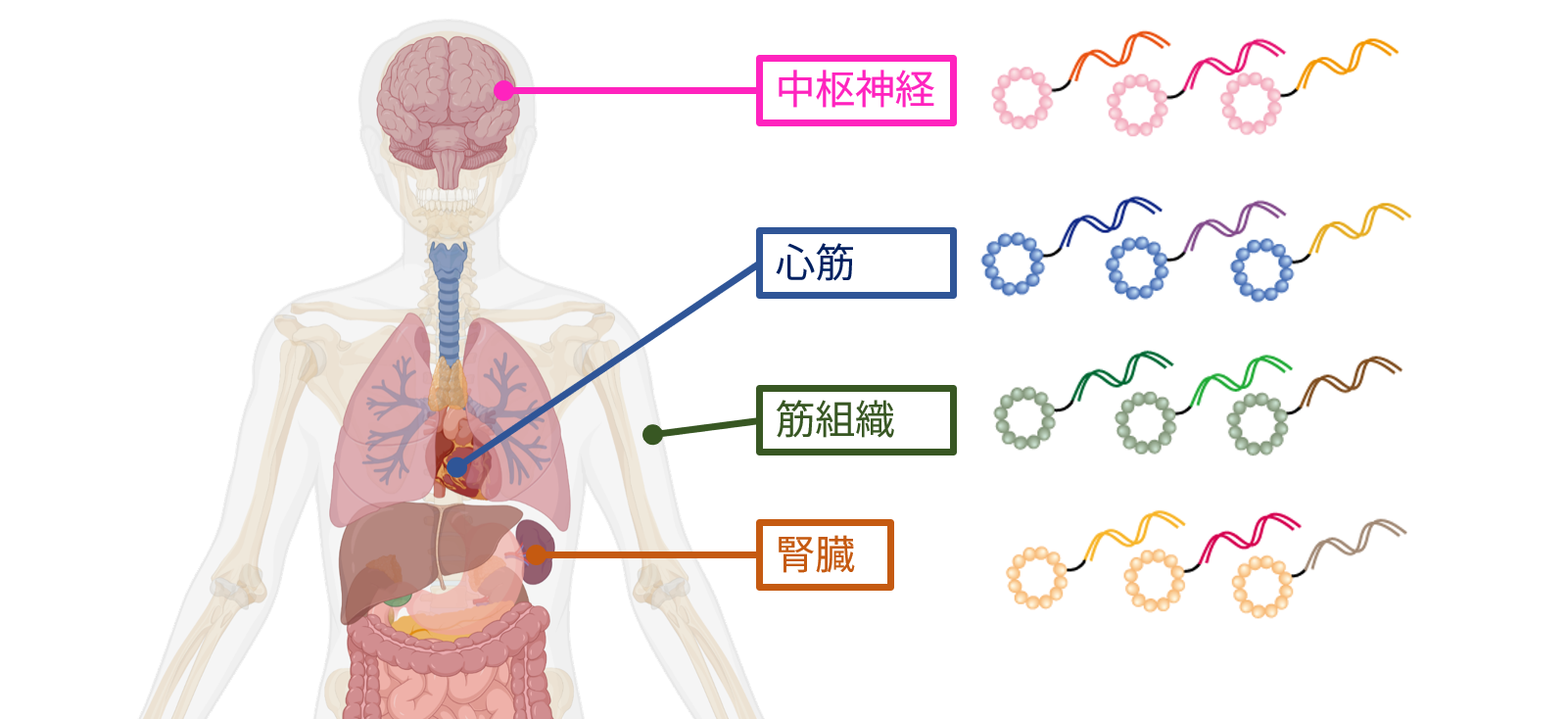
このように、核酸-PDCは非常に広がりのある領域であり、現在のペプチドリームにおけるRI-PDC領域のように、大きな柱へと育っていく可能性を秘めています。今後も、この核酸-PDC領域についての進捗もお知らせしていきたいと思います。

